二つの物質、例えば、高分子と溶媒、高分子と無機物質等を混ぜ合たい場合には、各々の物質の親和性が近いほど良く、解ける、溶解します。この親和性を大まかに判断する指標として、溶解度パラメータが利用できます。ここでは、溶解度パラメータを利用した物質の溶解性等を具体的な実例を紹介します。
物質間の親和性の尺度を表すものとして、溶解度パラメーターδ (溶解性パラメーター、Solubility Parameters、SP値) があり、類似した溶解度パラメーターを有した物資どうしは混ざりやすい。
溶解度パラメーターには、以下の種類があり、1-パラメーターのHiderbrand、3-パラメーターのHansenが一般的に使用されている。
1-パラメーターモデル : 1950年にHiderbrandが提唱
δ = {(⊿H - RT) / V }1/2、⊿H:蒸発のエンタルピー、V:モル容積
2-パラメーターモデル : 1964年にPrausnitz & Blanksが提唱
3-パラメーターモデル : 1967年にHansenが提唱
δ2 = δd2 + δp2 + δh2
δd:分散力による寄与項、δp:極性相互作用による寄与項、δh:水素結合による寄与項
単位 : (cal/cm-3)1/2 = 0.48888 x (MPa)1/2
(MPa)1/2 = (J/cm-3)1/2 = 2.0455 x (cal/cm-3)1/2
代表的な物資の25℃の溶解度パラメーター[(MPa)1/2]を下表に示す。提案者により若干数値が異なるが、相対値として使用する場合には実用的には問題はなさそう。 その他の化合物の溶解度パラメータは、別表(工事中)に示す。
| 物質名 | Hansen | Jayasri | Hoy | Burrell | δd | δp | δh |
| 水 |
47.8 | - | 48.0 | - | 15.6 | 16.0 | 42.3 |
| アルコール類:メタノール |
29.2 | 30.7 | 29.7 | 29.7 | 15.1 | 12.3 | 22.3 |
| エタノール |
26.4 | 26.5 | 26.1 | 26.0 | 15.8 | 8.8 | 19.4 |
| 1-プロパノール |
24.5 | 24.7 | 24.9 | 24.3 | 16.0 | 6.8 | 17.4 |
| 2-プロパノール(IPA) |
23.5 | - | - | - | 15.8 | 6.1 | 16.4 |
| 1-ブタノール | 23.5 | 23.7 | 23.3 | 23.1 | 16.0 | 5.7 | 15.8 |
| 1-ペンタノール | 21.7 | 22.4 | 22.8 | 22.3 | 16.0 | 4.5 | 13.9 |
| 1-ヘキサノール | 21.9 | 22.1 | 22.0 | 21.9 | 15.8 | 4.3 | 13.5 |
| 脂肪族:メタン | 9.6 | 9.5 | - | - | δd | δp | δh |
| エタン | 11.6 | 11.6 | - | - | δd | δp | δh |
| プロパン | 12.7 | 13.2 | 11.8 | - | δd | δp | δh |
| ヘキサン | 14.8 | 14.8 | 14.8 | - | 14.9 | 0 | 0 |
| シクロヘキサン | 16.7 | 16.8 | 16.8 | 16.8 | 16.8 | 0 | 0 |
| 芳香族:ベンゼン | 18.7 | 18.7 | 18.7 | 18.8 | 18.4 | 0 | 2.0 |
| トルエン | 18.2 | 18.3 | 18.3 | 18.2 | 18.0 | 1.4 | 2.0 |
| o-キシレン | 18.4 | 18.1 | 18.5 | 18.4 | 17.8 | 1.0 | 3.1 |
| m-キシレン | 18.0 | 18.3 | 18.2 | 18.0 | δd | δp | δh |
| p-キシレン | 17.9 | 18.0 | 18.1 | 17.9 | δd | δp | δh |
| その他:アセトン | 20.0 | 19.8 | 19.7 | 20.5 | 15.5 | 10.4 | 7.0 |
| アセトニトリル | 24.0 | 24.5 | 26.0 | 24.3 | 15.3 | 18.0 | 6.1 |
| アニリン | 22.6 | 21.3 | 21.9 | - | 19.4 | 5.1 | 10.2 |
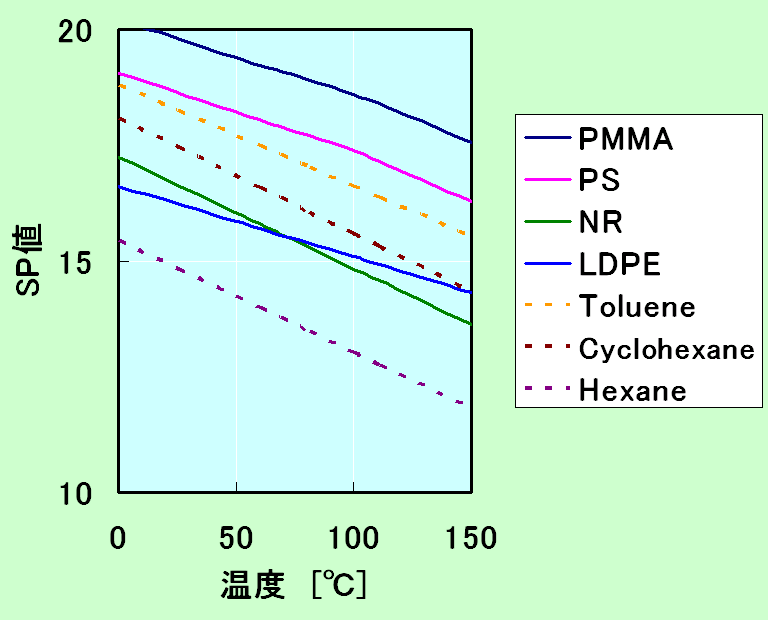
〇溶解度パラメータは、温度、圧力等の条件によりモル容積が変化するに伴い、変化するが、明確な関係式が確立していない。温度上昇に伴い溶解度パラメーターは小さくなり、圧力の上昇に伴い溶解度パラメーターは大きくなる。
◎温度の影響を表す式の例を以下に示す。
δ = δ0 + m x T {CRC, p303}
δ = δg + mi (T-Tg) {Malaysian Journal of Chemistry, 7, p57 (2005)}
◎圧力の影響を表す式の例を以下に示す。
δ = 8.09 x Pc0.5 x (ρr / ρl ) {CRC, p329}
Pc : 臨界圧力 (=7.38MPa@CO2)
ρr : 換算密度 (密度/臨界密度 =密度/468@CO2)
ρl : 標準状態の密度 (@ normal boiling point) (=2.66@CO2)
Hiderbrand溶解度パラメーターと<Hansen溶解度パラメーターの推算法は各種報告されており、基本的には、凝集エネルギー密度が置換基の種類及び数に依存していると考えるグループ寄与法を用い、以下の式と置換基種毎の定数が提示されている。
δ = [ ∑Ecoh / V ] 1/2
例 : Fedor
δ2 = δd2 + δp2 + δh2 = (∑Ed / V) + (∑Ep / V) + (∑Eh / V)
例 : Hoy
置換基の種類による上記例の推算法の凝集エネルギー密度、モル容積などを別ページ(工事中)に示す。
「溶解する」とは? :溶媒(Solvent)は通常、液体である。液体と気体の違いは液体では分子同士の相互作用が大きく、分子同士が離れずに密に存在していることである。そのような溶媒に溶質(Solute)が溶けこむ時、溶媒分子間に働く引力に割りこんで、溶質分子が入りこむことになる。もし、このとき、それぞれの分子同士の引き合う力が同程度であればお互いによく混ざり合うが、もし両者の引力が大きく異なると、溶媒分子同士あるいは溶質分子同士で集まってしまい均一な溶液にならないこととなる。
上記の考え方より、各々の物質の親和性が近いほど良く、解ける、溶解するので、この親和性を大まかに判断する指標として、溶解度パラメータが利用できる。
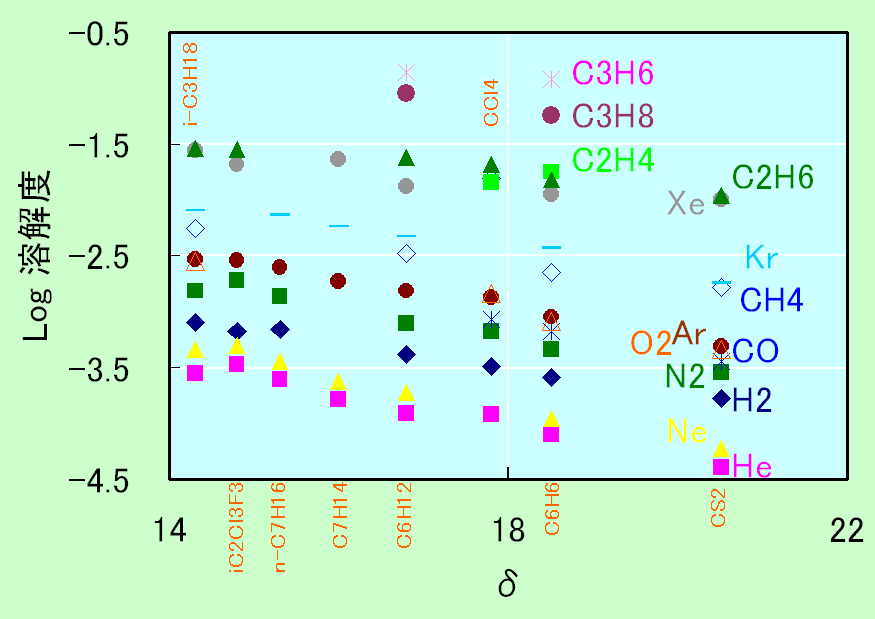
種々の気体の25℃、1気圧での溶解度と液体のSP値(横軸=δ)の関係を左図に示す。但し、テトラフルオロメタン、六フッ化硫黄の液体は直線性を示さない、又、二酸化炭素(CO2)の四塩化炭素(δ=17.8)、トルエン(δ=18.2)、ベンゼン(δ=18.5)への溶解度は、直線に載らないとの事{CRC p326}。これは、CO2(δ=17.3)とこれらの溶媒との電荷移動系相互作用のため直線性を示さないと考えられている。混合溶媒中への各種ガスの溶解度の推定に本手法が適用できるが、実液での確認が必要である。
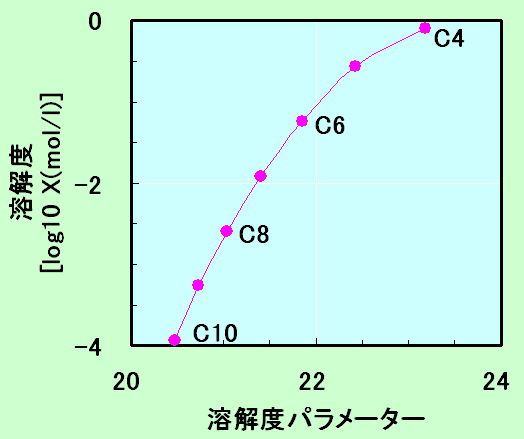
直鎖アルコールと水の相互溶解度は、アルコール分子の炭化水素が1つ増加する毎に等比級数的に減少するのが一般的である。アルコールのSP値を横軸に取るとその相関性が右図のように示される。
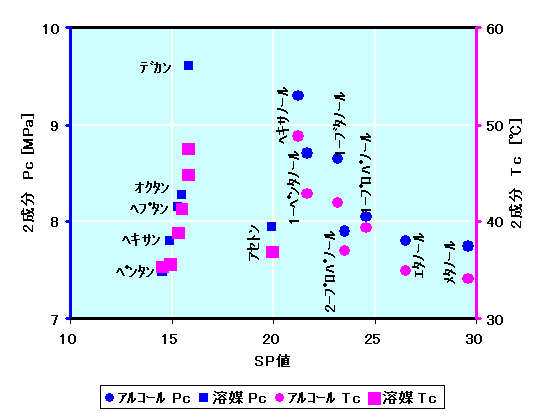
超臨界CO2へ各種アルコール、溶媒が2mol%溶解する時の2成分系の臨界圧力(Pc)と臨界温度(Tc)を縦軸に取り、横軸に各種アルコール、溶媒のSP値を示したものを右図に示す。
例えば、超臨界CO298mol%とエタノール(δ=26.5)2mol%の混合流体は、Pc=7.8MPa以上、Tc=35℃以下で完全相溶(ひとつの相)となり、その逆では、液液の二つの相となる。
脂肪族炭化水素(ペンタン~デカン)の2成分系のPcとTcは、超臨界CO2のSP値(δ=4.8 @ 8MPa,40℃)から離れる、大きくなるにつれて大きな値になる。一方、アルコールは、逆に炭素数が多くなる(SP値が小さくなる)と2成分系のPcとTcが多きくなる。これは、アルコールの-OH基とCO2のインターラクションが小さくなるからと考える。
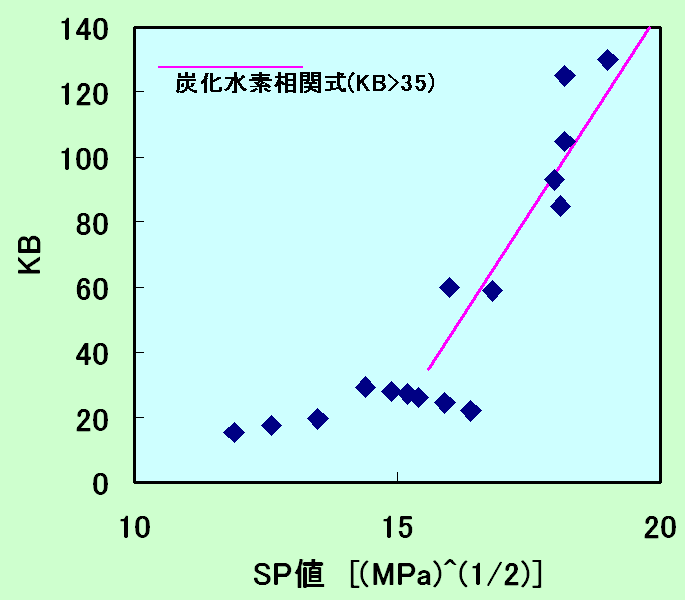
(a)KB値 (カウリブタノール値)
KB値は、溶剤の溶解能、即ち、脱脂力を示すもので、天然のカウリガムをブタノールで溶解させた溶液中への溶剤の溶解量で示すもので、この値が大きいほど溶解力の強い溶剤(洗浄剤)であることを示す。
Hansenは、溶媒中での高分子の溶解性を評価する方法として、以下R(i,j)が小さいとき、高分子と溶媒の物理的および化学的性質が類似し、その溶媒中での高分子の溶解性が高いと提案している。
R(i,j) = [ 4 (δd,i - δd,j)2 + (δp,i - δp,j)2 + (δh,i - δh,j)2]1/2
(a)ポリマーブレンド(2種類のポリマーを混ぜる)
SP値が近ければ相溶性の均一なポリマー構造になるが、SP値が離れていれば「海島構造」になりがちである。
(b)ポリマーの耐薬品性
ポリマーがどのような薬品に対して抵抗力があるかの目安となり、SP値の近い溶剤は親和性が高いために材料内に浸透しやすい。
(c)異種ポリマーのヒートシール(加熱による接着)
SP値が近いポリマーほど、熱接着しやすい傾向がある。
一次粒子径が、0.2μmから6.8μmのα-Al2O2(0.5μm)、α-Fe2O3(0.7μm)、アナターゼ型TiO2(0.2μm)、La2O3(0.5μm)、Ce2O3(4.8μm)、Y2O3(6.8μm)の粒子の溶媒中での分散性に6項のポリマーと溶媒の溶解性パラメーターを適用し、固体粒子の溶解度パラメーターδp、δhは、それぞれ粒子の比誘電率の値および等電点の値と強い相関性があることを示した。{化学工学論文集, 28, p641 (2002)}
これを利用すると、ナノ粒子の分散性を高める溶媒選定への適用可能性がある。
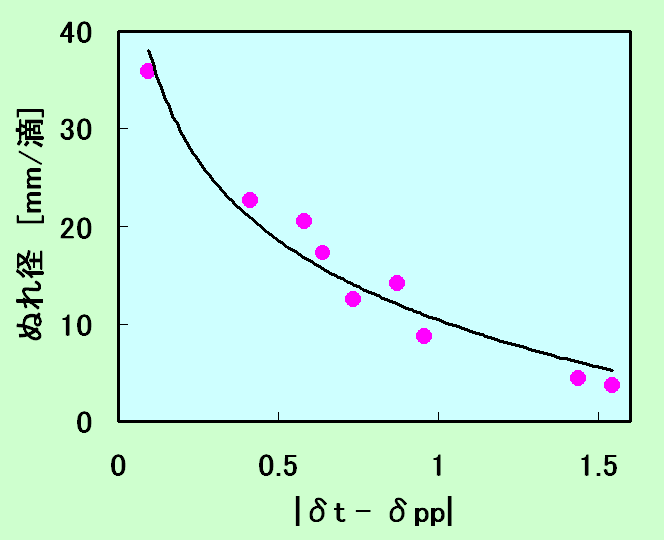
樹脂ファルム表面の溶媒での湿潤性、ぬれ性の評価指標としての使用例。PP(ポリプロピレン)フィルム上に一定容積の油(絶縁油)を滴下してその油滴の広がりによって判定したものを右図に示す。油のSP値(δt)とPPフィルムのSP値(δpp)が近似するほどぬれ性が良くなることを示している。{National Technical Report, 23, p228 (1977)}
** 参考文献 ** CRC : Handbook of Solybility Parameters and Other Cohesion Parameters, second Edition, A.F.M. Barton, CRC Press (1991)