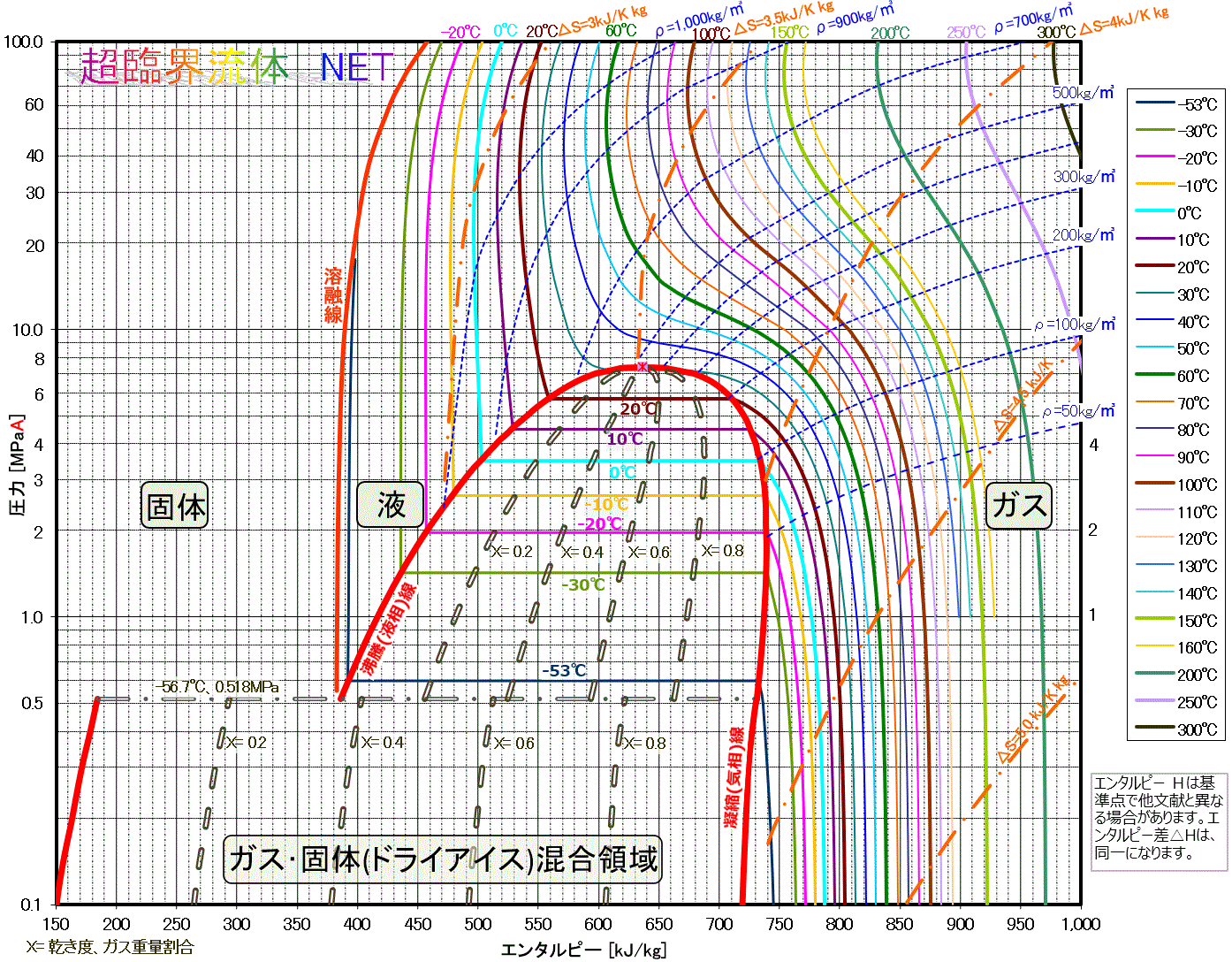
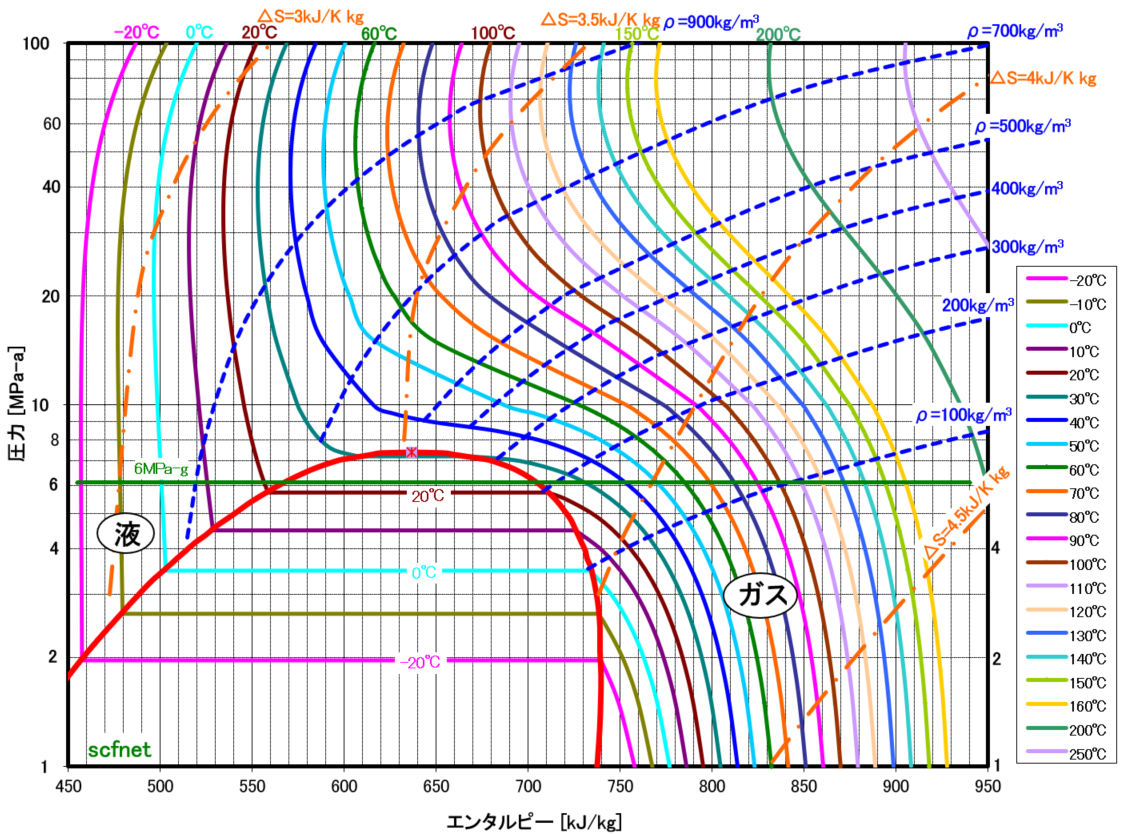
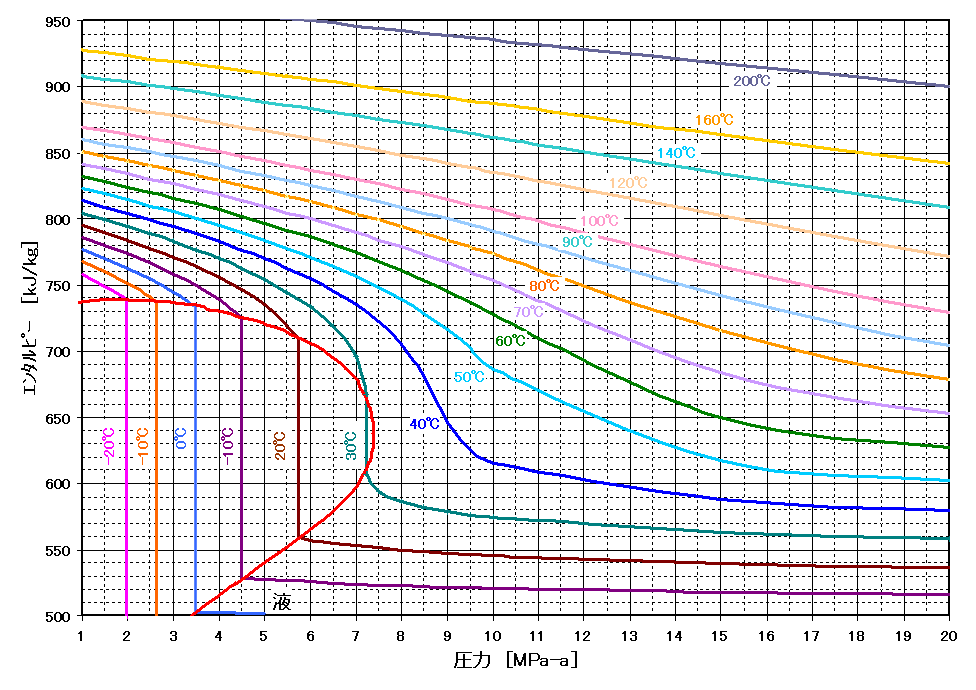
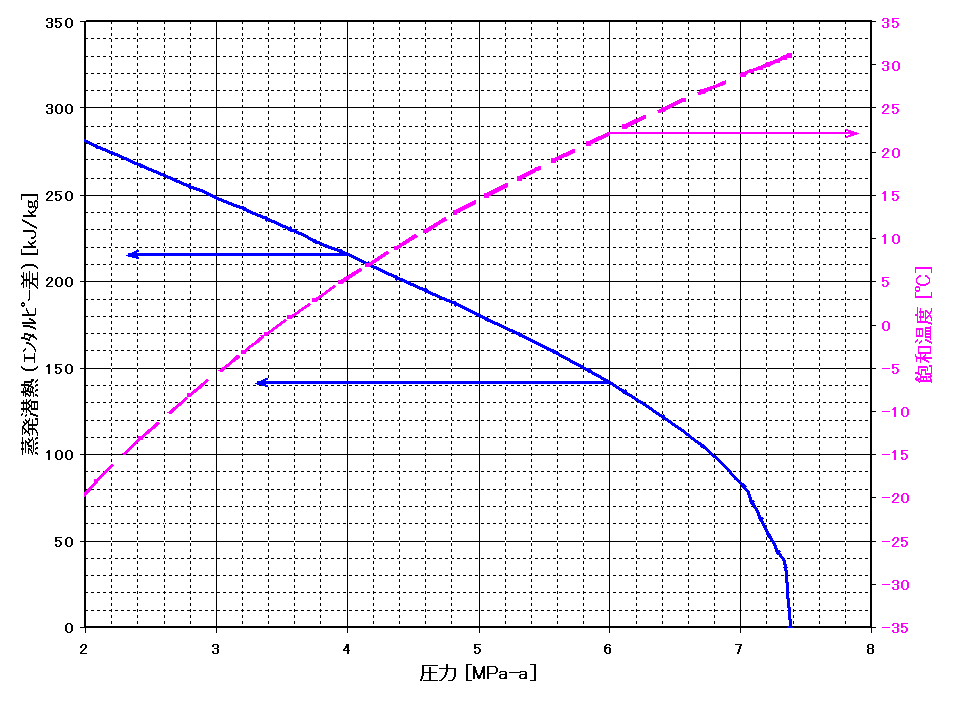
| 本ページ内の図等の構成 モリエル線図の説明・使い方 ・脱フロンCO₂液化プロセスの例 図1.エンタルピー vs 圧力(0.1MPa~、~200℃) 図5.エンタルピー vs 圧力(0.1MPa~、~500℃) 図6.ドライアイス領域含む エンタルピー vs 圧力(0.1MPa~、~200℃) 図7.エンタルピー vs 圧力(1MPa~、~160℃) 図8.圧力(1~20MPa) vs エンタルピー 図9.圧力 vs 蒸発潜熱 注記:1kgのCO₂が持っているエンタルピーを |
モリエル線図(p-h線図、圧力-比エンタルピー線図)は、縦軸に圧力、横軸にエンタルピー(CO₂の熱量)を取ったもので、超臨界CO₂サイクルでのCO₂の状態を表せます。操作条件の各種状態でのCO₂の状態を1枚の線図で描く事により、
各部の状態や数値を知り、また、その数値を使用して熱量計算や運転状態の判断に活用する事ができます。特に、プロセス・装置設計する場合には、二酸化炭素のエンタルピーの特長を理解して行うことが非常に重要です。 ・臨界点近傍では、圧力、温度の僅かな変化でエンタルピー、熱容量が大きく変化 ・二酸化炭素の蒸発潜熱は圧力が高い程小さくなり、液化温度は高くなり、液化しやすくなる。 一方、二酸化炭素中の不純物との分離は、圧力が低いほど、効率的になる。 二酸化炭素を回収、分離、液化して再利用する場合には、冷凍機の効率も含めて最適化する。 ⇒ 工業化:CO₂回収で詳細説明します。 超臨界CO₂のプロセス運転条件とモリエル線図の見方はこちらで詳細説明します。 |
モリエル線図で使用するエンタルピーは、熱力学的な物理量の一つで、定圧下でのエンタルピーの変化量は、その物質CO₂に出入りするエネルギーに等しく、加熱・冷却する熱交換器での交換熱量と等しくなります。
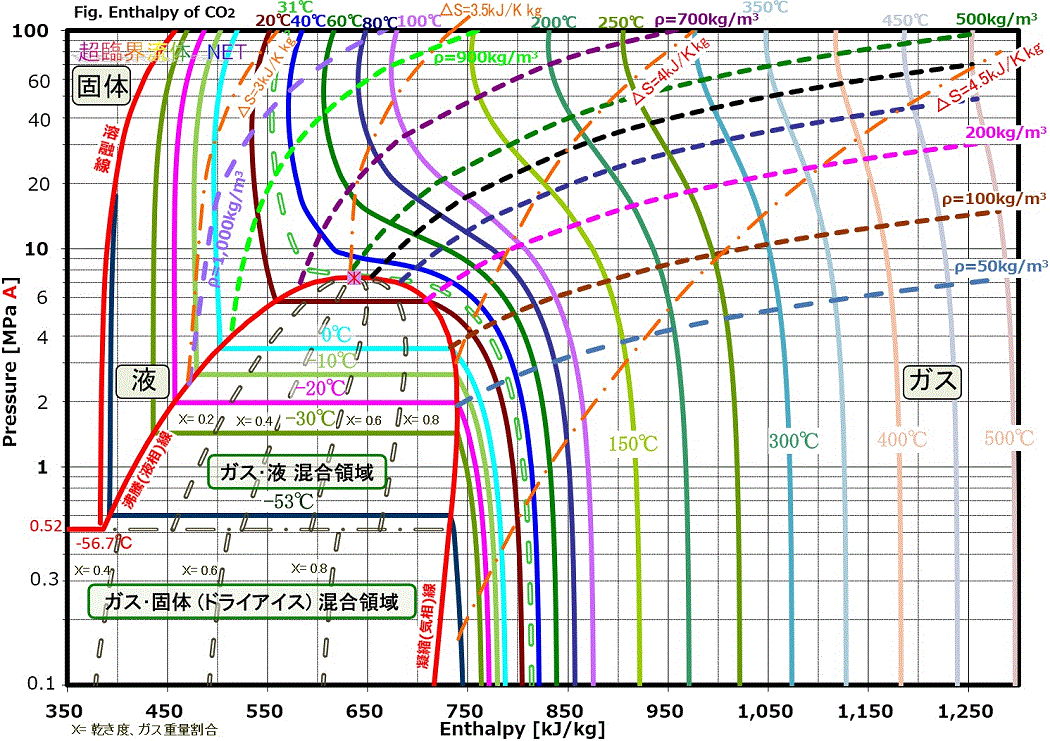
例えば、図1より、20MPa、20℃、537kJ/kg (図3. )のCO₂を20MPa、100℃に加熱するとエンタルピーは、729kJ/kg (図3.
)のCO₂を20MPa、100℃に加熱するとエンタルピーは、729kJ/kg (図3. )となり、CO₂加熱に必要な交換熱量は、192kJ/kgとなります。
)となり、CO₂加熱に必要な交換熱量は、192kJ/kgとなります。
図1に示すエンタルピーは、日本機械学会編:流体の熱物性値集(1983年8月発行)によります。これでの臨界点 7.3825MPaA、304.21K(31.06℃)のエンタルピーは、636.6 kJ/kgです。エンタルピーの基準点が異なると数値が異なりますが、差で利用しますので特に問題はありません。
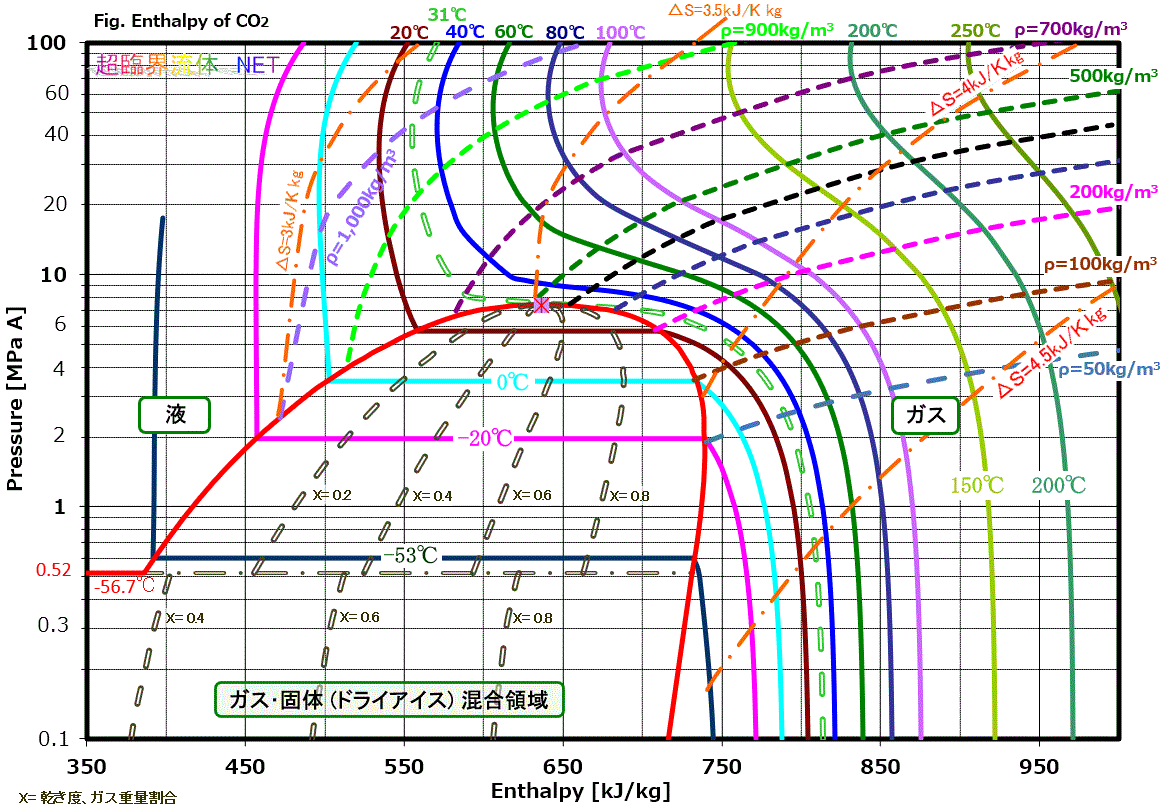
図1. CO₂モリエル線図


 )。加熱するとガスが発生しだし、
エンタルピーが増加し、定圧線に沿って右側に移行し、エンタルピーが739kJ/kg (図3.
)。加熱するとガスが発生しだし、
エンタルピーが増加し、定圧線に沿って右側に移行し、エンタルピーが739kJ/kg (図3. ) に達すると、液は全てガスになります。この時の蒸発熱=潜熱は、739-461= 278kJ/kgと計算できます。
) に達すると、液は全てガスになります。この時の蒸発熱=潜熱は、739-461= 278kJ/kgと計算できます。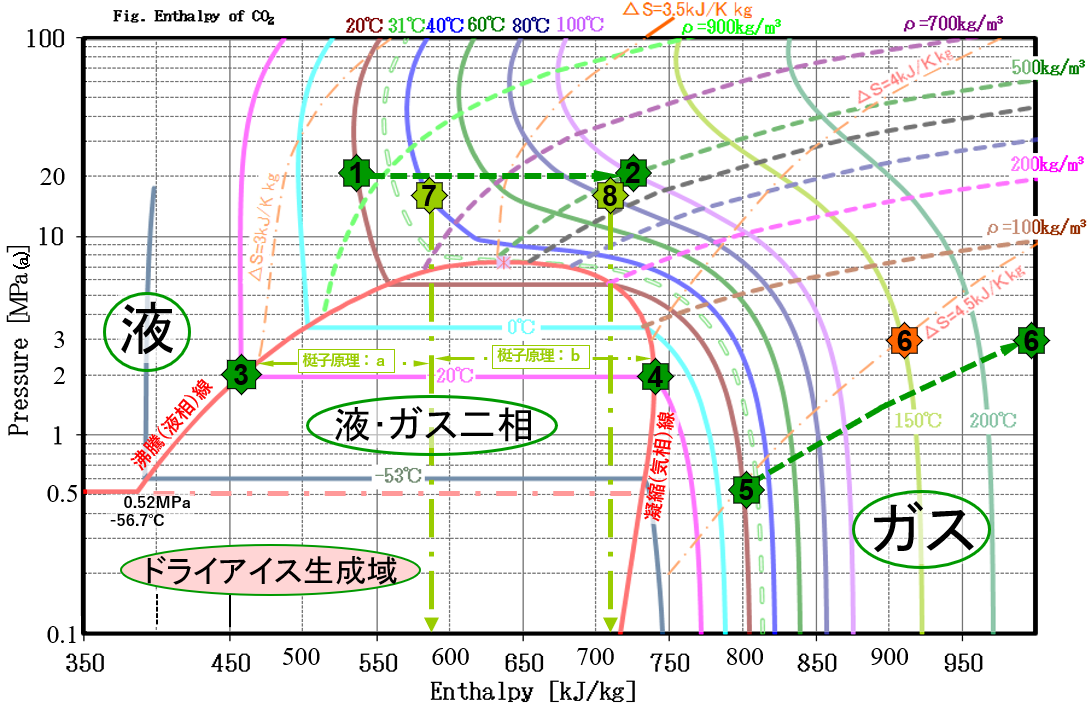
 )
から圧縮比5.3で3MPaAまで圧縮すると等エントロピー圧縮では148℃、907kJ/ kg (図3.
)
から圧縮比5.3で3MPaAまで圧縮すると等エントロピー圧縮では148℃、907kJ/ kg (図3. ) ですが、実際の圧縮では非可逆でエントロピーが増加し、断熱効率56%の時は、228℃、990kJ/kg
(図3.
) ですが、実際の圧縮では非可逆でエントロピーが増加し、断熱効率56%の時は、228℃、990kJ/kg
(図3. ) になります。
) になります。 )から真下に圧力が低下し、赤線の沸騰線を横切ると液とガスが共存する二相流域に入ります。
更に圧力が下がり、0.52MPaGになるとドライアイスが発生します。沸騰線以下で発生する液とガスの割合は、梃子原理()で計算します。例えば、2MPaG時に発生するガス量は、図3の梃子原理:a/(a+b)、液量は、梃子原理:b/(a+b)で、以下のようになります。
)から真下に圧力が低下し、赤線の沸騰線を横切ると液とガスが共存する二相流域に入ります。
更に圧力が下がり、0.52MPaGになるとドライアイスが発生します。沸騰線以下で発生する液とガスの割合は、梃子原理()で計算します。例えば、2MPaG時に発生するガス量は、図3の梃子原理:a/(a+b)、液量は、梃子原理:b/(a+b)で、以下のようになります。 )から、真下に変化し、2MPaG時で発生するガス・液量は以下となります。
)から、真下に変化し、2MPaG時で発生するガス・液量は以下となります。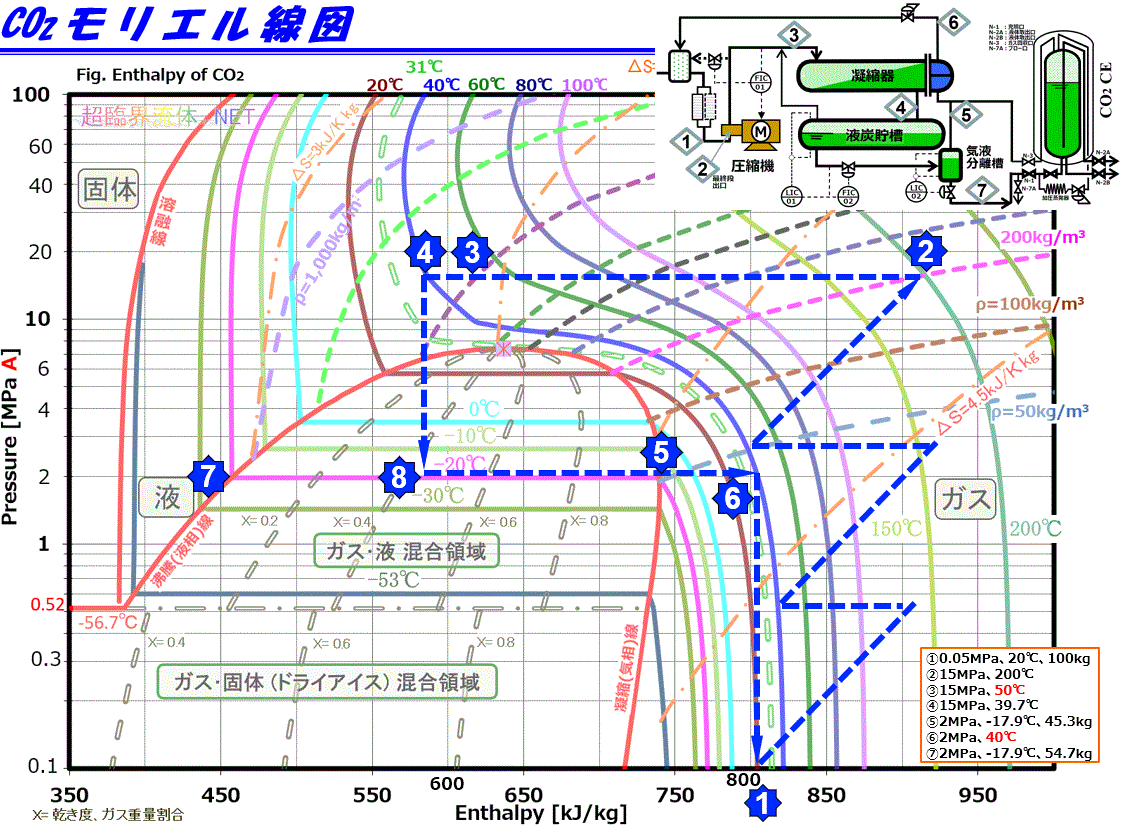
 から例えば3段で15MPa迄冷却水で冷却しながら圧縮した後
から例えば3段で15MPa迄冷却水で冷却しながら圧縮した後 (図4では200℃)、冷却水で50℃に冷却し
(図4では200℃)、冷却水で50℃に冷却し 、凝縮器で
、凝縮器で 状態から断熱膨張されたCO₂で40℃冷却する。
15MPa、40℃のCO₂をコールドエバポレータCE充填圧の2MPa迄断熱膨張する
状態から断熱膨張されたCO₂で40℃冷却する。
15MPa、40℃のCO₂をコールドエバポレータCE充填圧の2MPa迄断熱膨張する と54.7kg-液CO₂と45.3kg-ガスCO₂となり、液CO₂はCEに充填し、ガスCO₂は温度が-17.9℃と低いため、凝縮器で冷却水で50℃迄冷却された圧縮ガスを冷却し(フロン冷凍機の代替)40℃迄加温され、
大気圧に断熱膨張され20℃に降温し圧縮機の吸込みに戻ります。全体的な収支は以下となります:
と54.7kg-液CO₂と45.3kg-ガスCO₂となり、液CO₂はCEに充填し、ガスCO₂は温度が-17.9℃と低いため、凝縮器で冷却水で50℃迄冷却された圧縮ガスを冷却し(フロン冷凍機の代替)40℃迄加温され、
大気圧に断熱膨張され20℃に降温し圧縮機の吸込みに戻ります。全体的な収支は以下となります: = 圧縮機吸込CO₂ガス 100kg
= 圧縮機吸込CO₂ガス 100kg )kJ/kgx45.3kg
)kJ/kgx45.3kg